Muitos dos requisitos apresentados pelos sistemas eléctricos convencionais implicam desafios técnicos específicos para as células de combustível.
Por exemplo, de maneira a ter uma maior flexibilidade em relação ao combustível e melhor utilização do calor produzido, uma célula de combustível deverá funcionar a temperaturas elevadas.
De maneira a responder aos diversos desafios técnicos, os investigadores desenvolveram diferentes tipos de células de combustível.
Tabela de Conteúdos
Principais tipos de células de combustível
- Células de combustível com membrana de permuta protónica (CCMPP).
- Células de combustível alcalinas (CCA).
- Células de combustível ácido fosfóricas (CCAF).
- Células de combustível de carbonato fundido (CCCF).
- Células de combustível de óxido sólido (CCOS).
Tipo CCMPP – Célula de combustível com membrana de permuta protónica
A célula de combustível com membrana de permuta protónica apresenta a vantagem da sua simplicidade de funcionamento.
O electrólito nesta célula de combustível é uma membrana de permuta iónica (polímero ácido sulfónico fluorizado ou outro polímero similar) que é boa condutora de protões do ânodo para o cátodo. Por sua vez, o combustível utilizado é o hidrogénio com elevado grau de pureza [Kordesch et al., 1996].
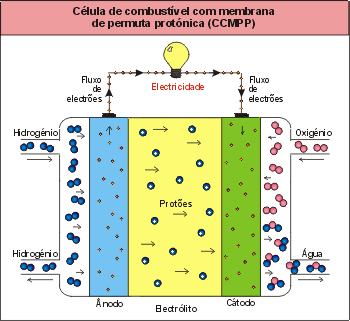
O único líquido na célula é a água e, devido a esse facto, os problemas de corrosão são mínimos [Cappadonia et al., 2000].
A presença da água líquida na célula é de extrema importância porque a membrana de permuta protónica deve ser mantida hidratada durante o funcionamento da célula de combustível.
Devido às limitações apresentadas em relação à temperatura, impostas pelo polímero da membrana e pela necessária da hidratação da membrana, esta célula de combustível funciona para temperaturas, usualmente, inferiores a 100º Centígrados [Cappadonia et al., 2000].
Sendo assim, as velocidade de reacção reduzidas são compensadas pela utilização de catalisadores e eléctrodos sofisticados.
O catalisador utilizado é a platina e desenvolvimentos recentes permitiram a utilização de pequenas quantidades de catalisador, sendo o custo da platina uma pequena parte no preço total da CCMPP.
Para além do hidrogénio como combustível, as células de combustível CCMPP podem funcionar com combustíveis alternativos (células de combustível indirectas), desde que estes sejam previamente convertidos em hidrogénio. Os combustíveis utilizados é CCMPP indirectas podem ser, por exemplo, metanol, etanol, metano, propano, etc..
Uma variante importante da CCMPP é a célula de combustível com alimentação directa de metanol (CCDM). Como combustível, o metanol tem diversas vantagens em relação ao hidrogénio – para além de ser líquido à temperatura ambiente, este pode ser facilmente transportado e armazenado [Hirschenhofer et al., 1998].
Os principais problemas das CCDM são o sobrepotencial electroquímico no ânodo, o que torna a célula menos eficiente, e o facto do metanol difundir através da membrana de permuta protónica (MPP) do ânodo para o cátodo.
No entanto, no presente, os investigadores desta tecnologia estão a alcançar progressos importantes que resolvem parcialmente estes problemas, tornando este tipo de células de combustível potencialmente útil para ser utilizado em equipamentos eléctricos portáteis e, igualmente, em meios de transporte [Larminie, 2002].
| Reacções CCMPP | Reacções CCDM |
| Ânodo: H2(g) -> 2 H+(aq) + 2 e– Cátodo: 1/2 O2(g) + 2 H+(aq) + 2 e– -> H2O(l) |
Ânodo: CH3OH(aq) + H2O(l) -> CO2(g) + 6 e– + 6 H+(aq) Cátodo: 6 H+(aq) + 6 e– + 3/2 O2(g) -> 3 H2O(l) |
.
Tipo CCA – Céulas de combustível alcalinas
Nas células de combustível alcalinas, o electrólito utilizado é uma solução concentrada de KOH (85 %peso) para temperaturas elevadas (~ 250 ºC) e menos concentrada (35 – 50 %peso) para temperaturas interiores (< 120 ºC) [Larminie, 2002].
As pilhas CCA utilizadas no programa Apollo da NASA utilizavam uma solução de KOH com 85 %peso e funcionavam à temperatura de 250 ºC [Kordesch et al., 1996].
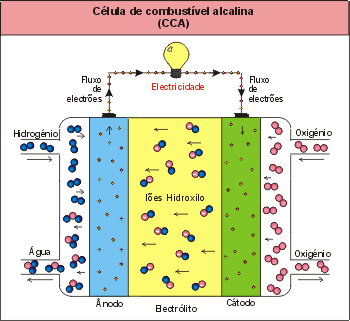
O problema das velocidades de reacção baixas (baixas temperaturas) é superado com a utilização de eléctrodos porosos, com platina impregnada, e com a utilização de pressões elevadas.
Neste tipo de células de combustível, a redução do oxigénio no cátodo é mais rápida em electrólitos alcalinos, comparativamente com os ácidos e, devido a isso, existe a possibilidade da utilização de metais não nobres neste tipo de células [Larminie, 2002].
As principais desvantagens desta tecnologia são o facto dos electrólitos alcalinos (p. ex. NaOH e KOH) dissolverem o CO2 e a circulação do electrólito na célula, tornando o funcionamento desta mais complexo [Larminie, 2002].
No entanto o electrólito apresenta custos reduzidos.
| Reacções CCA |
| Ânodo: H2(g) + 2 OH–(aq) -> 2 H2O(l) + 2 e– Cátodo: 1/2 O2(g) + H2O(l) + 2 e– -> 2 OH–(aq) |
Tipo CCAF – Céulas de combustível de ácido fosfórico
As células de combustível ácido fosfóricas foram as primeiras a ser produzidas comercialmente e apresentam uma ampla aplicação a nível mundial. Muitas unidades de 200 kW, produzidas pela empresa “International Fuel Cells Corporation” estão instaladas nos Estados Unidos e na Europa [Larminie, 2002].
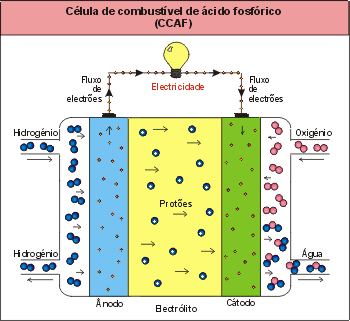
Neste tipo de células de combustível, o electrólito utilizado é o ácido fosfórico a ~100%, funcionando a temperaturas entre 160 ºC e 220 ºC.
Para temperaturas baixas, o ácido fosfórico é um mau condutor iónico e o envenenamento da platina pelo CO no ânodo torna-se mais severo.
A estabilidade relativa do ácido fosfórico é elevada em comparação com outros ácidos comuns e, consequentemente, a célula de combustível CCAF pode produzir energia eléctrica a temperaturas elevadas (220 ºC).
Para além disso, a utilização de um ácido concentrado (~100 %) minimiza a pressão de vapor da água, facilitando a gestão da água na célula.
O suporte utilizado universalmente para o ácido é o carboneto de silicone e o electrocatalisador utilizado no ânodo e cátodo é a platina [Kordesch et al., 1996].
O problema do armazenamento do hidrogénio pode ser resolvido pela transformação do metano em hidrogénio e dióxido de carbono, mas o equipamento necessário para esta operação acrescenta à célula custos consideráveis, maior complexidade, e tamanho superior [Larminie, 2002].
No entanto, estes sistemas apresentam as vantagens associadas à simplicidade de funcionamento da tecnologia das células de combustível, disponibilizando um sistema de produção de energia eléctrica seguro e que envolve baixos custos de manutenção.
Alguns destes sistemas funcionaram continuamente durante diversos anos sem qualquer necessidade de manutenção ou intervenção humana [Larminie, 2002].
| Reacções CCAF |
| Anodo: H2(g) -> 2 H+(aq) + 2 e– Cátodo: 1/2 O2(g) + 2 H+(aq) + 2 e– -> H2O(l) |
Tipo CCCF – Céulas de combustível de carbonato fundido
A célula de combustível de carbonato fundido utiliza como electrólito uma combinação de carbonatos alcalinos (Na, K, Li), que são estabilizados num suporte de LiAlO2.
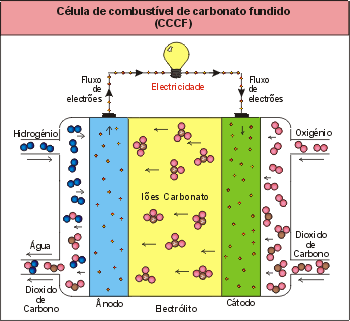
Este tipo de células de combustível funciona na gama de temperaturas entre 600 e 700 ºC, para as quais os carbonatos alcalinos formam um sal altamente condutor de iões (ião carbonato).
Para temperaturas elevadas pode-se utilizar o níquel como catalisador no ânodo e óxido de níquel no cátodo, não sendo necessária a utilização de metais nobres [Hirschenhofer et al., 1998].
Devido às temperaturas elevadas de operação, neste tipo de sistema pode utilizar-se directamente gás natural, não havendo a necessidade da utilização de “reformadores” externos.
No entanto, esta simplicidade é contraposta pela natureza do electrólito, uma mistura quente e corrosiva de lítio, potássio e carbonatos de sódio.
| Reacções CCCF |
| Ânodo: H2(g) + CO32- -> H2O(g) + CO2(g) + 2 e– Cátodo: 1/2 O2(g) + CO2(g) + 2 e– -> CO32- |
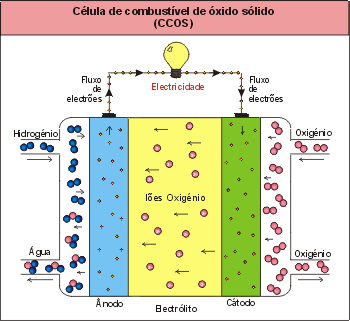
Tipo CCOS – Céulas de combustível de óxido sólido
As células de combustível de óxido sólido funcionam na gama de temperaturas entre os 600 ºC e os 1000 ºC, possibilitando assim velocidades de reacção elevadas sem a utilização de catalisadores nobres [Hirschenhofer et al., 1998].
O electrólito utilizado neste tipo de célula é um metal óxido, sólido e não poroso, usualmente Y2O3-estabilizado em ZrO2. Na gama de temperaturas elevadas de funcionamento, os iões de oxigénio são transportados do ânodo para o cátodo.
O metano pode ser utilizado directamente, não sendo necessária a utilização de uma unidade de reformação externa [Larminie, 2002].
No entanto, os materiais cerâmicos que constituem estas células acarretam dificuldades adicionais na sua utilização, envolvendo custos de fabrico elevados e sendo necessários muitos equipamentos extra para que a célula produza energia eléctrica.
Este sistema extra engloba o de pré aquecimento do combustível e do ar, e o sistema de arrefecimento. Apesar de funcionar a temperaturas superiores a 1000 ºC, o electrólito da CCOS mantém-se permanentemente no estado sólido.
Tipicamente o ânodo é Co-ZrO2 ou Ni-ZrO2 e o cátodo é Sr-LaMnO3 [Kordesch et al., 1996].
| Reacções CCOS |
| Ânodo: H2(g) + O2- -> H2O(l) + 2 e– Cátodo: 1/2 O2(g) + 2 e– -> O2- |
Leitura Recomendada: Células de Combustível – Como Funcionam




